
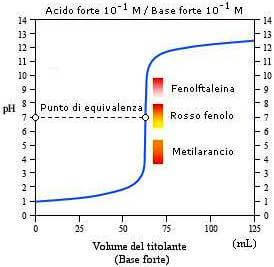
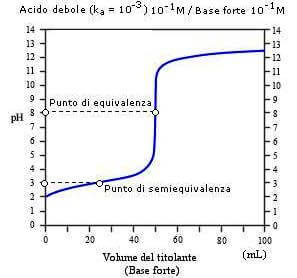
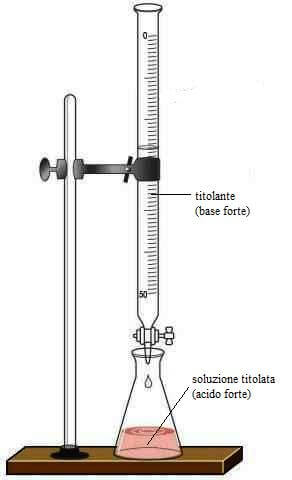
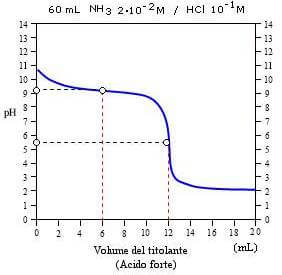
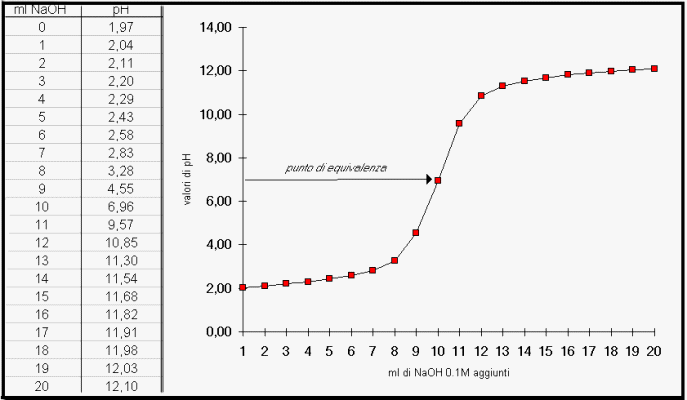
Analisi Volumetrica Titolazioni acido-base Un acido può essere titolato con una soluzione standard di base e viceversa acido forte - base forte H + (aq) - ppt scaricare

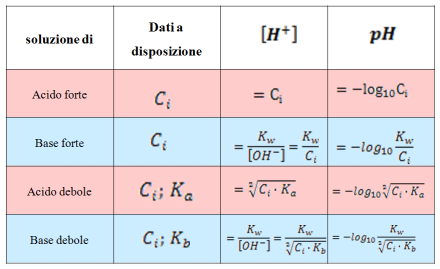
Il pH della soluzione di un sale Caso I: Sali di acido forte e base forte (es. NaCl) 1)NaCl → Na + + Cl - (dissociazione completa) 2)Na + + 2H 2 O ↛ H. - ppt scaricare






.png)

